
Vai ter Prouni no segundo semestre de 2026?
Isabella Baliana | 10/06/26Descubra se o Prouni será realizado no segundo semestre de 2026 e saiba quem pode se inscrever para concorrer às bolsas de estudo.
Saiba o que é o metanol, por que ele é tão tóxico e como o tema pode ser abordado no Enem e em outros vestibulares.
Em resumo:
A seguir, entenda por que o metanol é tão perigoso, qual a diferença pro etanol e ainda veja exemplos de exercícios que já caíram no exame.
Recentemente, o metanol ganhou destaque no Brasil devido a diversos casos de intoxicação causados por bebidas alcoólicas adulteradas. A relevância do tema também fez com que o metanol se tornasse um ponto de interesse para quem se prepara para o vestibular.
Encontre bolsas de estudo de até 80%
O metanol, um composto químico altamente tóxico, já foi abordado em questões do Enem, que exigem dos candidatos conhecimento sobre os impactos das substâncias no organismo humano.

O que estudar para Química no Enem?
+ Gabarite a prova de Ciências da Natureza do Enem com essas 5 dicas
O metanol (CH₃OH), também chamado de álcool metílico, é um composto orgânico utilizado principalmente como solvente industrial e combustível.
Mas, afinal, por que ele é tão perigoso? De acordo com Michel Arthaud, que leciona Química na Plataforma Professor Ferretto, a principal “armadilha” do metanol está em sua semelhança inicial com o etanol. “O metanol é um álcool simples, assim como o etanol. A grande diferença está no que o nosso organismo faz com essas duas moléculas”, explica.
O fígado humano produz uma enzima chamada álcool desidrogenase (ADH), responsável por iniciar a metabolização de qualquer tipo de álcool. É neste ponto que a tragédia começa. “A enzima ADH não é muito seletiva. Ela oxida tanto o etanol quanto o metanol, iniciando o processo de quebra dessas moléculas”, detalha.
Propanol, metanol e propano: o que são, diferenças e fórmulas estruturais
+ Funções Orgânicas: entenda o grupo funcional hidrocarboneto
Enquanto a metabolização do etanol gera subprodutos que o corpo consegue eliminar com relativa segurança, o mesmo não acontece com o metanol. “O metanol é oxidado e se converte em formaldeído pela enzima ADH. E, imediatamente, outra enzima transforma esse formaldeído em ácido fórmico. E é esse ácido fórmico o grande vilão da história”, alerta o professor.
O ácido fórmico é uma substância extremamente ácida e tóxica. Seu acúmulo no sangue causa uma condição chamada acidose metabólica severa, que ataca principalmente o sistema nervoso, incluindo o nervo óptico.
“É por isso que um dos sintomas clássicos da intoxicação por metanol é a cegueira. O ácido fórmico destrói o nervo óptico. Em doses mais altas, leva ao coma e à parada cardiorrespiratória”, ressalta.
O etanol (C2H6O), também conhecido como álcool etílico, é o tipo de álcool encontrado em bebidas alcoólicas e é considerado seguro para consumo, desde que em doses moderadas. Já o metanol é utilizado em processos industriais e não tem aplicação alimentícia, sendo extremamente perigoso quando ingerido.
A principal diferença entre os dois compostos está na forma como o corpo os metaboliza. O etanol é convertido no fígado em acetato, que é utilizado como fonte de energia pelo organismo.
Por outro lado, o metanol é convertido em formaldeído, um composto altamente venenoso, e em ácido fórmico, que pode levar à acidez sanguínea grave, prejudicando vários sistemas do corpo.
Essa diferença crucial é o motivo pelo qual o metanol nunca deve ser consumido, ao contrário do etanol, que é amplamente consumido, especialmente em bebidas alcoólicas.
Sim, o metanol pode ser abordado em questões do Enem, especialmente na área de Ciências da Natureza, mas não porque o assunto ficou em alta. O composto pode cair porque o exame frequentemente explora questões relacionadas a substâncias químicas e seus efeitos no corpo humano.
Assim, o metanol pode aparecer de várias maneiras, trazendo desde perguntas sobre suas propriedades até discussões sobre a forma como ele pode ser metabolizado pelo corpo humano e os riscos associados ao seu consumo.
Além disso, o metanol pode cair em questões que se relacionem com:
A seguir, confira algumas questões que envolviam o metanol e já caíram no Enem e em outros vestibulares:
1 – Enem (2012)
Um dos métodos de produção de biodiesel envolve a transesterificação do óleo de soja utilizando metanol em meio básico (NaOH ou KOH), que precisa ser realizada na ausência de água. A figura mostra o esquema reacional da produção de biodiesel, em que R representa as diferentes cadeias hidrocarbônicas dos ésteres de ácidos graxos.
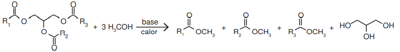
A ausência de água no meio reacional se faz necessária para:
a) manter o meio reacional no estado sólido.
b) manter a elevada concentração do meio reacional.
c) manter constante o volume de óleo no meio reacional.
d) evitar a diminuição da temperatura da mistura reacional.
e) evitar a hidrólise dos ésteres no meio reacional e a formação de sabão.
2 – Unicamp (2023)
Com o objetivo de mitigar problemas ambientais e encontrar alternativas viáveis para a produção de combustíveis, muitas propostas têm sido sugeridas. As figuras a seguir mostram rotas de transformação que possibilitariam alcançar o objetivo citado:
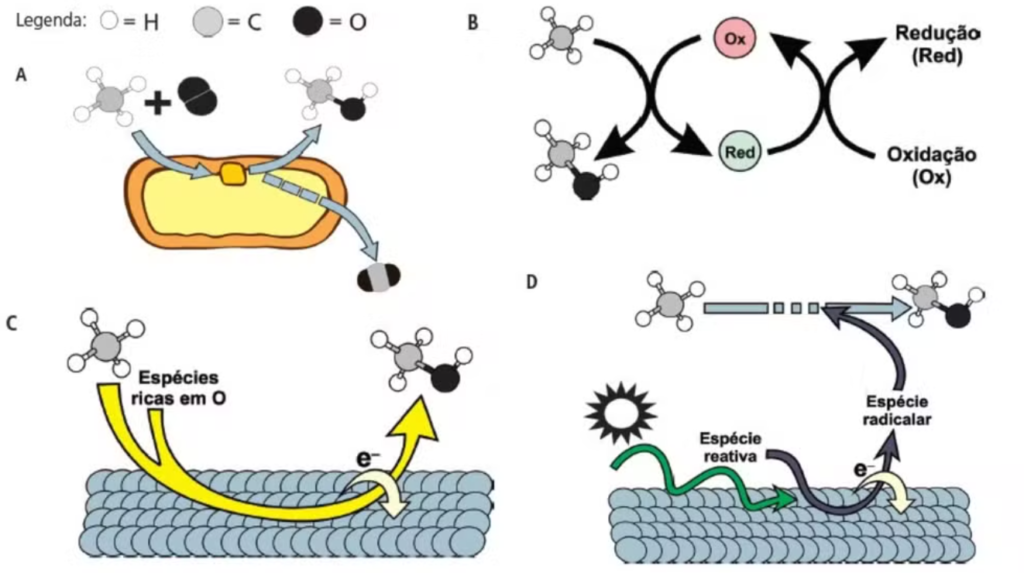
As figuras anteriores trazem a representação esquemática de diferentes sistemas catalíticos para a reação de transformação de:
a) dióxido de carbono em etanol, sendo que A, B, C e D representam, respectivamente: biocatálise, catálise homogênea, catálise heterogênea e fotocatálise.
b) dióxido de carbono em etanol, sendo que A, B, C e D representam, respectivamente: biocatálise, catálise homogênea, fotocatálise e catálise heterogênea.
c) metano em metanol, sendo que A, B, C e D representam, respectivamente: biocatálise, catálise homogênea, catálise heterogênea e fotocatálise.
d) metano em metanol, sendo que A, B, C e D representam, respectivamente: biocatálise, catálise homogênea, fotocatálise e catálise heterogênea.
3 – Univesp (2021)
A reação de síntese mais utilizada para a formação do metanol (CH₃OH), um biocombustível muito utilizado nas indústrias químicas como solvente, ocorre a partir da reação entre os gases monóxido de carbono (CO) e hidrogênio (H₂). A equação não balanceada que representa a reação é:
CO (g) + H₂ (g) —> CH₃OH (ℓ)
Em uma reação de síntese do metanol, com 100% de rendimento, foi empregado 25 g de hidrogênio gasoso e quantidade suficiente de monóxido de carbono.
A quantidade máxima de metanol produzida nessa síntese é igual a:
a) 50 g.
b) 100 g.
c) 200 g.
d) 400 g.
e) 800 g.
Respostas:
1 – E
2 – C
3 – C
O Preparadão Enem chegou para ajudar quem está estudando para o Enem e busca uma preparação intensiva e focada para a prova.
No Preparadão, você tem acesso ao guia de redação, um plano de estudos completo e organizado com exercícios e resumos, além de diversas dicas e materiais extras, sem cobrar nada por isso.
Se você quiser tudo isso, basta entrar para a comunidade clicando no botão abaixo:
Está de olho na oportunidade de estudar e quer saber como fazer isso pagando mensalidades mais em conta?
A Quero Bolsa, uma plataforma que oferece bolsas de estudo de até 80% em mais de 1.000 instituições de ensino espalhadas por todo o Brasil, pode ajudar você a transformar isso em realidade.
Se você se interessou e quer saber mais sobre como ela funciona, confira abaixo alguns artigos e entenda melhor como conseguir uma bolsa!
Confira abaixo algumas das melhores instituições de ensino do Brasil que são parceiras da Quero Bolsa e aproveitar as ofertas disponíveis.